play.jpg
0
untitled.jpg
0
STORYBOARD RANCANGAN MEDIA PEMBELAJARAN SMAMENGGUNAKAN MCROSOFT POWER POINT
0STORYBOARD RANCANGAN MEDIA PEMBELAJARAN SMA
MENGGUNAKAN MCROSOFT POWER POINT BERPENDEKATAN CTL
Disusun oleh : Falasifah Aulia
4301410044
Pendidikan Kimia 2010
STORYBOARD RANCANGAN MEDIA PEMBELAJARAN SMAMENGGUNAKAN MCROSOFT POWER POINT
0STORYBOARD RANCANGAN MEDIA PEMBELAJARAN SMA
MENGGUNAKAN MCROSOFT POWER POINT BERPENDEKATAN CTL
Disusun oleh : Falasifah Aulia
4301410044
Pendidikan Kimia 2010
|
No. SK : 1. Memahami struktur atom, sifat-sifat periodic unsur, dan ikatan kimia No. KD : 1.2 Membandingkan proses pembentukan ikatan ion, ikatan kovalen, ikatan kovalen koordinasi, dan ikatan logam serta hubungannya dengan sifat fisik senyawa yang terbentuk Indikator: Menyelidiki kepolaran bebrapa senyawa dan hubungannya dengan keelektronegatifan melalui percobaaan
No. Scene : 1-18 Scenes |
|||||
|
No |
Gambar |
Keterangan |
|||
|
1. |
|
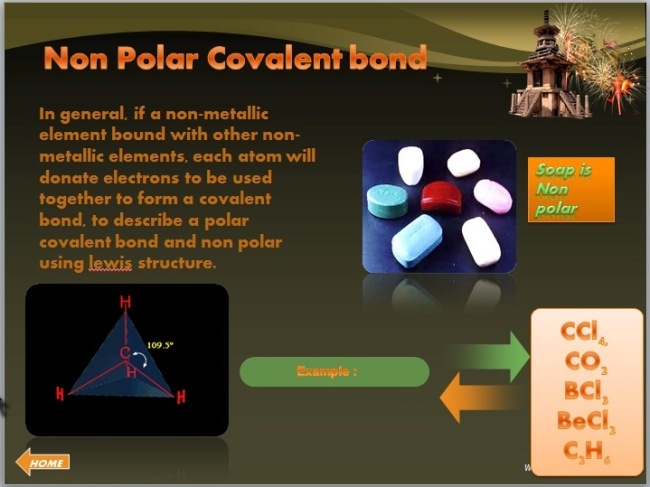
Pada slide pertama merupakan halaman judul yang berisi judul dari materinya, yaitu Polar and Non Polar Bond dengan disertai gambar-gambar yang berhubungan dengan materi.
|
|||
|
2. |
|
Pada slide berikutnya terdapat tampilan yang menunjukkan identitas pemilik media beserta nama UNNES. |
|||
|
3.
|
|
Pada tampilan berikutnya yaitu terdapat menu utama yang berisi link untuk menuju ke menu-menu berikutnya, yaitu introduction, material, evaluasi, serta penutup (closing), yaitu introduction (sk, kd, pokok bahasan, serta indikator), material (kepolaran, ikatan kovalen polar, ikatan kovalen non polar), Evaluation ( berisi 5 soal yang akan diujikan ), Closing ( berisi thank you ), dan disetiap slide akan berisi tombol HOME untuuk kembali ke menu utama.
|
|||
|
4. |
|
Pada introduction terdapat 4 menu yang pertama berisi standart kompetensi, kemudian kompetensi dasar, pokok bahasan, serta indicator pencapaian. |
|||
|
5. |
|
Slide berikutnya adalah penjelasan mengenai keelektronegatifan berdasarkan skala Pauling |
|||
|
6. |
|
Slide berikutnya berisi tentang materi kepolaran, dimana disitu dijelaskan mengenai kepolaran berdasarkan perbedaan keelektronegatifan |
|||
|
7
|
|
Slide berikutnya masih sama dengan slidfe sebelumnya, yaitu menjelaskan tentang kepolaran
. |
|||
|
8 |
Tampilan ini mengenai materi ikatan kovalen polar beserta aplikasinya dalam kehidupan sehari-hari |
||||
|
9 |
|
Pada slide ini sama dengan slide sebelumnya, yaitu penjelasan mengenai ikatan kovalen polar. |
|||
|
10 |
|
Pada slide ini menjelaskan materi kovalen non polar beserta contoh aplikasi yang nyata dalam kehidupan sehari-hari |
|||
|
11 |
|
Slide berikutnya yaitu penjelasan mengenai kovalen non polar, yaitu mengenai kekuatan gaya tolak antara pasangan electron bebas denganterikat, serta pasangan electron terikat dan terikat. |
|||
|
12 |
Pada slide ini berisi tentang penjelasan tentang gaya tarik menarik antara dua molekul polar. |
||||
|
13 |
|
Di slide ini berisikan contoh-contoh aplikasi nyata dari senyawa kovalen polar dan non polar dalam kehidupan sehari-hari. |
|||
|
14 |
|
Pada slide ini berisi tentang eksperiment atau contoh simulasi untuk menentukan sifat larutan termasuk polar atau non polar dengan menggunakan penggaris yang sudah digosok-gosokan pada kain wol. |
|||
|
15 |
|
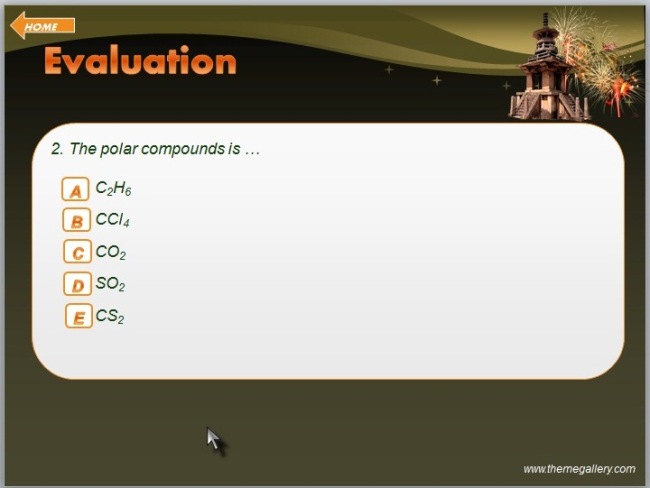
Slide berikutnya berisi evaluasi, pada menu evaluasi ini berbentuk tampilan kotak dengan disertai penomoran yang bertujuan sebagai pemilihan nomor soal, denga menggunakan kotak-kotak seperti siswa akan dibagi menjadi 3 kelompok besar yang masing-masing akan menjawab pertanyaan dengan memilih nomer yang ada pada kotak tersebut secara bergantian,setiap kelompok ketika menjawab pertanyaan juga disertakan dengan alasan pemilihan jawaban. Setiap menjawab benar maka akan muncul smile yang menandakan benar, dan ketika jawabannya salah maka tampilan yang muncul adalah tampilan sedih. Selain soal dalam permainan tersebut juga tersedia bom serta bonus, ada 3 nomer yang berisi bonus da nada 3 nomer juga yang berisi bom. |
|||
|
16 |
Slide berikutnya berisi soal evaluasi |
||||
|
17 |
|
Slide berikutnya berisi sama yaitu soal, ada 14 slide yang berisi soal hingga slide ke-29 . |
|||
|
18 |
Slide berikutnya adalah slide icon sedih yang menandakan jika jawaban yang dipilih adalah salah, namun slide ini hanya akan terlihat ketika melakukan permainan evaluasi tersebut. |
||||
|
19 |
Pada slide ini berisi tampilan gambar yang menunjukan bonus, yaitu ketika memilih nomer pada slide evaluasi dengan permainan, namun slide ini hanya akan terlihat ketika melakukan permainan evaluasi tersebut. |
||||
|
20 |
Pada slide ini yang muncul adalah tampilan bom, yaitu ketika memilih nomer pada kotak evaluasi dengan permainan. |
||||
|
21 |
Pada slide ini adalah tampilan untuk smile bahagia karena menjawab pertanyaan dengan benar, sama tampilan ini juga hanya akan muncul ketika melakukan permainan. |
||||
|
22 |
Slide yang terakhir yang akan muncul setelah penyampaian materi serta melakukan evaluasi adalah ucapan terimakasih dengan sedikit kata motivasi, yaitu “If you believe you can, be sure that you can do it”. |
||||
STORYBOARD RANCANGAN MEDIA PEMBELAJARAN SMAMENGGUNAKAN MCROSOFT POWER POINT
0
STORYBOARD RANCANGAN MEDIA PEMBELAJARAN SMA
MENGGUNAKAN MCROSOFT POWER POINT BERPENDEKATAN CTL
Disusun oleh : Falasifah Aulia
4301410044
Pendidikan Kimia 2010
|
No. SK : 1. Memahami struktur atom, sifat-sifat periodic unsur, dan ikatan kimia No. KD : 1.2 Membandingkan proses pembentukan ikatan ion, ikatan kovalen, ikatan kovalen koordinasi, dan ikatan logam serta hubungannya dengan sifat fisik senyawa yang terbentuk Indikator: Menyelidiki kepolaran bebrapa senyawa dan hubungannya dengan keelektronegatifan melalui percobaaan
No. Scene : 1-18 Scenes |
|||||
|
No |
Gambar |
Keterangan |
|||
|
1. |
|
Pada slide pertama merupakan halaman judul yang berisi judul dari materinya, yaitu Polar and Non Polar Bond dengan disertai gambar-gambar yang berhubungan dengan materi.
|
|||
|
2. |
|
Pada slide berikutnya terdapat tampilan yang menunjukkan identitas pemilik media beserta nama UNNES. |
|||
|
3.
|
|
Pada tampilan berikutnya yaitu terdapat menu utama yang berisi link untuk menuju ke menu-menu berikutnya, yaitu introduction, material, evaluasi, serta penutup (closing), yaitu introduction (sk, kd, pokok bahasan, serta indikator), material (kepolaran, ikatan kovalen polar, ikatan kovalen non polar), Evaluation ( berisi 5 soal yang akan diujikan ), Closing ( berisi thank you ), dan disetiap slide akan berisi tombol HOME untuuk kembali ke menu utama.
|
|||
|
4. |
|
Pada introduction terdapat 4 menu yang pertama berisi standart kompetensi, kemudian kompetensi dasar, pokok bahasan, serta indicator pencapaian. |
|||
|
5. |
|
Slide berikutnya adalah penjelasan mengenai keelektronegatifan berdasarkan skala Pauling |
|||
|
6. |
|
Slide berikutnya berisi tentang materi kepolaran, dimana disitu dijelaskan mengenai kepolaran berdasarkan perbedaan keelektronegatifan |
|||
|
7
8
|
|
Slide berikutnya masih sama dengan slidfe sebelumnya, yaitu menjelaskan tentang kepolaran
Tampilan ini mengenai materi ikatan kovalen polar beserta aplikasinya dalam kehidupan sehari-hari. |
|||
|
9 |
|
Pada slide ini sama dengan slide sebelumnya, yaitu penjelasan mengenai ikatan kovalen polar. |
|||
|
10 |
|
Pada slide ini menjelaskan materi kovalen non polar beserta contoh aplikasi yang nyata dalam kehidupan sehari-hari |
|||
|
11 |
|
Slide berikutnya yaitu penjelasan mengenai kovalen non polar, yaitu mengenai kekuatan gaya tolak antara pasangan electron bebas denganterikat, serta pasangan electron terikat dan terikat. |
|||
|
12 |
Pada slide ini berisi tentang penjelasan tentang gaya tarik menarik antara dua molekul polar. |
||||
|
13 |
|
Di slide ini berisikan contoh-contoh aplikasi nyata dari senyawa kovalen polar dan non polar dalam kehidupan sehari-hari. |
|||
|
14 |
|
Pada slide ini berisi tentang eksperiment atau contoh simulasi untuk menentukan sifat larutan termasuk polar atau non polar dengan menggunakan penggaris yang sudah digosok-gosokan pada kain wol. |
|||
|
15 |
|
Slide berikutnya berisi evaluasi, pada menu evaluasi setiap menjawab benar maka akan muncul smile yang menandakan benar, dan ketika jawabannya salah maka tampilan yang muncul adalah smile sedih. |
|||
|
16 |
Slide berikutnya berisi evaluasi |
||||
|
17 |
|
Slide berikutnya berisi evaluasi |
|||
|
18 |
Slide terakhir yaitu ucapan terima kasih. |
||||
Love Myspace Calendar – Red Hearts
00
MODULE OF
PERIODIC SYSTEM ELEMENTS
MATERIALS
1.DEVELOPMENT OF PERIODIC SYSTEM
Atom has a very small mass. The method of determining the relative atomic mass stated by Berzelius (1814) from Sweden and P. Dulong and A. Petit (1819), both from France. Berzelius and Dulong and Petit determine the relative atomic mass of the element based on specific heat. The relative atomic mass of an element essential nature and a specific nature, as each element has a specific relative atomic mass different from the other elements.
1.1. Based on metal characteristic, elements divided become metal and nonmetal.
| The elements classified as |
metals and as
nonmetals
1.2.Triade Dobereiner
In 1829, Johan Wolfgang Dobereiner, a professor of chemistry in Germany, suggests that the relative atomic mass of Strontium is very close to the average mass of the two other elements like Litium, Natrium and Kalium that. Dobereiner also found some other elements such groups. Therefore, Dobereiner conclude that the elements can be grouped into groups called “Triade tiga unsur”. But unfortunately, Dobereiner failed to show enough triade so useful rule. Although the idea of Dobereiner not very successful, but it is the first at tempt in the classification of the element. The theory of Dobereiner, example :
|
Element |
Atomic mass |
Atomic mass in the middle |
|
Li
Na
K |
6,94
22,94
39,10 |
Atomic mass Na = Atomic mass Li + Atomic mass K 2 = 6,94 + 39,10 = 23,02 2
|
1.3.Newlands law of octaves
In 1864 a British chemist named AR Newlands announced the discovery of the so-called Law of Octaves. Newlands arrange the elements of increasing relative atomic mass. Ex. law of octaves Newland is as follows:
| Element | Atomic number |
| Li | 1 |
| Be | 2 |
| B | 3 |
| C | 4 |
| N | 5 |
| O | 6 |
| F | 7 |
| Na | 8 |
| Mg | 9 |
| Al | 10 |
| Si | 11 |
| P | 12 |
| Cl | 13 |
| K | 14 |
| Ca | 15 |
Newlands law of octaves proved valid only for light elements, roughly up to calcium (Ar=40). If passed, similar properties proved too forced.
1.4.Mendeleev Periodic System
In 1869 a Russian scholar named Dmitri Ivanovich Mendeleev, based on observations of 63 elements known at the time, concluded that the properties of elements are a periodic function of the relative atomic mass. That is, if the elements are arranged according to their relative atomic mass increases, the specific properties will be repeated periodically. Mendeleev placed elements that have similar properties in a single vertical column, called Group. Rows of horizontal, ie lane elements of increasing relative atomic mass, called the period.
1.5.Modern Periodic System of Henry G.Moseley
In the early 20th century, our knowledge of the atom has developed very basic. The experts found that the atom is not something that is not divided but a particle composed of smaller particles called elementary particles or subatomic particles. Atom is now believed to consist of three types of elementary particles, ie protons, electrons, and neutrons. For now we need to mention that the number of protons is characteristic of the element, meaning that each element has a specific number of protons different from other elements. The number of protons in an atom is called the atomic number.
| Figure 1 |